1.4 Химическая коррозия. Газовая коррозия#
Многие металлические конструкции подвергаются коррозионному разрушению при воздействии на них сухих газов (воздуха, продуктов горения топлива при высоких температурах и др.), а также жидких неэлектролитов (нефть, бензин, жидкая сера, бром и др.). В этом случае протекает гетерогенная химическая реакция газообразной или жидкой среды с металлом, при которой окисление металла и восстановление окислительного компонента коррозионной среды протекают в одном акте. Это химическая коррозия.
Химическая коррозия возникает при взаимодействии металла (Ме) с агрессивным компонентом коррозионной среды (X).
Ме + X → МеX (продукт коррозии).
Продукты коррозии образуются непосредственно на поверхности металла. Механизм химической коррозии сводится к диффузии атомов или ионов металла сквозь постепенно утолщающуюся пленку продуктов коррозии и встречной диффузии атомов или ионов газа или жидкости. Скорость и характер химической коррозии определяется, поэтому, свойствами возникающих пленок.
Наиболее распространенным видом химической коррозии является газовая коррозия – это коррозия металлов в газах при высоких температурах.
Газовая коррозия имеет место при высокотемпературной обработке металлов (ковка, штамповка, прокатка, термообработка и др.), а также при эксплуатации многих металлических изделий (газовые турбины, печи, котлы, химические аппараты, теплообменники, двигатели внутреннего сгорания и др.).
Металл в процессе химической коррозии выступает в роли восстановителя, он отдает электроны и окисляется. Компонент агрессивной среды выступает в роли окислителя, акцептора электронов. В процессе реакции он восстанавливается. В роли окислителей могут быть О2, Сl2, НСl, SO2, CO2 и т.д.
Для большинства процессов основным условием осуществления химической коррозии является отсутствие на поверхности металла пленки воды.
Типичными примерами химической коррозии металлов являются реакции их взаимодействия с кислородом при высокой температуре (газовая коррозия):
$$ 2Me + \frac{1}{2}n\cdot O_{2} = Me_{2}O_{n} \text{при n=1,3,5,7;} $$
$$ Me + \frac{1}{4}n\cdot O_{2} = MeO_{\frac{n}{2}} \text{при n=2,4,6,8;} $$
где n - валентность металла.
Суммарный процесс коррозии металлов с галогенами и серой описывается следующими формулами:
$$ \text{с галогенами}\qquad\qquad Me + nГ = MeГ_{n}\left(Г = F_{2}, Cl_{2}, Br_{2}, I_{2} \right) $$
$$ \text{с серой}\qquad\qquad Me + nS = Me_{2}S_{n}\quad \text{при n = 1, 3, 5, 7;} $$
$$ Me + \frac{1}{2}nS = Me_{\frac{n}{2}}\quad \text{при n= 2, 4, 6, 8.} $$
В среде, содержащей углерод и азот, при высокой температуре возможно окисление металлов с образованием карбидов МеmCn и нитридов MemNn.
Влияние температуры на скорость газовой коррозии#
Температура является одним из наиболее важных факторов, от которых зависит скорость перехода в окисленное состояние. С ростом температуры скорость реакции увеличивается, подчиняясь экспоненциальной зависимости в соответствии с уравнением Аррениуса.
$$ k = A \cdot e^{\frac{-E_{a}}{RT}} $$
где k – константа скорости реакции;
А – нормирующий множитель;
T – абсолютная температура, К;
R – универсальная газовая постоянная;
Еа – энергия активации.
Состав среды также оказывает большое влияние на скорость газовой коррозии металлов. Особенно сильно влияют кислород, соединения серы и водяные пары.
Жаростойкость – способность металлов сопротивляться газовой коррозии.
Жаропрочность – способность металлов сохранять механические свойства при высоких температурах.
Металл может быть жаростоек, но не жаропрочен и наоборот. Многие алюминиевые сплавы жаростойки, но не жаропрочны. Наоборот, быстрорежущая сталь Р18 – жаропрочна, но не жаростойка. Хорошие сочетания жаростойкости и жаропрочности у сплавов на основе Ni, Cr, Co.
Железо и его сплавы, при высоких температурах, покрываются смесью оксидов железа, называемых железной окалиной.
В состав окалины может входить:
- вюстит – закись железа FeO, обычно встречается в виде минерала. Он имеет гранецентрированную кубическую решетку. Оксид имеет хорошую ионную и электронную проводимость. Вюстит не обладает защитными свойствами.
- магнетит – закись-окись железа Fe3O4. Магнетит имеет сложную кристаллическую решетку типа шпинели. Он является ферромагнетиком. Защитные свойства выше, чем у вюстита.
- гематит – оксид железа Fe2O3, прилегающий к магнетиту и имеющий такую же кристаллическую решетку и свойства магнетита. Имеет две кристаллические модификации: α – Fe2O3 и γ – Fe2O3.
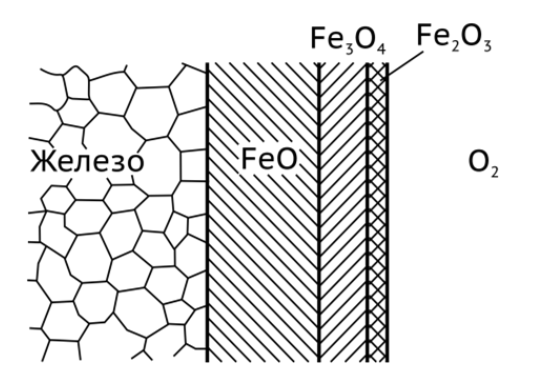
Непосредственно к металлу примыкает закись железа FeO, далее следуют Fe3O4 и Fe2O3. Соотношение толщин оксидов FeO : Fe3O4 : Fe2O3 близко к 100:10:1.